Il 4 gennaio 1961 moriva Erwin Schrödinger, premio Nobel per la Fisica 1933, considerato uno degli scienziati più influenti del secolo scorso.

Il diciannovesimo secolo fu non solo un trampolino formidabile per le scoperte fisiche e ingegneristiche del 1900, ma diede anche i natali a moltissime figure fondamentali per lo sviluppo della tecnica e della ricerca. Fra questi anche Erwin Schrödinger, nato a Vienna il 12 Agosto 1887.
Un gatto e un fisico entrano in un bar
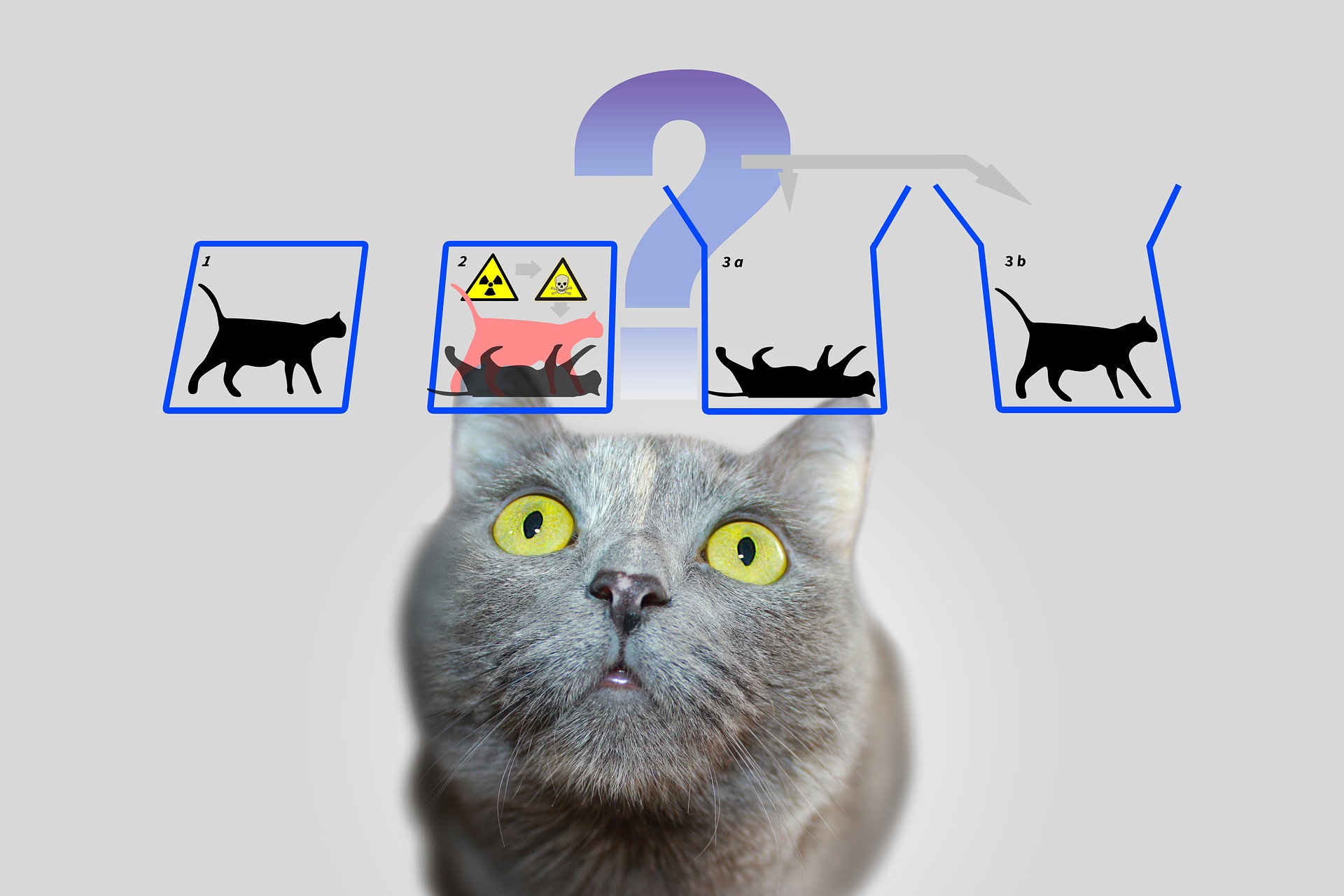
Se potessimo riassumere la vita di Erwin Schrödinger con una barzelletta, probabilmente inizierebbe così. Per nostra fortuna Schrödinger preferiva la fisica alla comicità. Dimostratosi molto portato per la matematica e la fisica già da ragazzo, ottenne un dottorato in fisica e collaborò con scienziati del calibro di Einstein, Fermi e Planck. Nipote di un professore di chimica, crebbe in una famiglia agiata, sebbene non ricca, che seppe sempre garantirgli gli studi. Subì influenze di diversi maestri, tra cui Friedrich Hasenöhrl, che morì nella Grande Guerra, a cui anche Schrödinger prese parte. Si sposò a 33 anni e fu un uomo per così dire tumultuoso anche dal punto di vista amoroso: ebbe numerose amanti e molti figli. Si può dire che prese alla lettera la famosa frase “la monogamia non è naturale”, attribuita al suo coevo e amico Albert Einstein. Ma cosa ha a che fare un gatto con la fisica quantistica? Andando avanti con il tempo, la ricerca scopre fenomeni e formula concetti sempre più complicati e difficilmente fruibili. Fortunatamente Schrödinger e altri suoi colleghi erano non solo geniali, ma anche ottimi oratori propensi alla diffusione della conoscenza. Questo fu un fatto che li distinse profondamente da altri giganti del passati quali ad esempio Newton, consapevole della sua enorme intelligenza e sprezzante nei confronti del mondo intero. Per questa ragione si trovavano spesso a dover spiegare ad allievi, cariche politiche e altri ancora, difficili teorie nel modo più semplice possibile. Nonostante negli anni il paradosso del gatto abbia subito diversi attacchi e accuse di essere incoerente o troppo semplificato, esso rimane comunque uno degli esempi più famosi e illustri di spiegazione della meccanica quantistica in termini semplici. Schrödinger lega la vita di un gatto in una scatola ad un evento ben più imprevedibile: il decadimento di un elemento radioattivo. Prima di tutto è necessario dare una breve definizione di decadimento. Pensate agli atomi come ad una vostra zia che fa la spesa: i protoni sono il suo peso, i neutroni sono i gioielli che porta al braccio e al collo, mentre gli elettroni le buste della spesa una volta uscita dal supermercato. Fino a che la zia è in forma, non indossa molti gingilli e acquista poca spesa, nessun problema si presenta, e può tornare a casa con ciò che ha comperato. Dopo qualche mese invece arrivano le norme per evitare la diffusione del coronavirus. Allora la zia sta in casa, prende peso e le poche volte che esce vuole sfoggiare il suo intero portagioie. Immaginatevi la spesa ora: la zia fa scorta e quindi acquista più prodotti, ha qualche chilo in più e anche difficoltà a muoversi per tutti i gioielli che indossa. Il risultato è semplice: o lascia qualche articolo in cassa o rischia di perdere qualche pendente per strada o, soluzione più radicale, perde peso. Quando gli atomi comincia ad esserci troppo ingombro accade lo stesso. Così avviene il decadimento, ossia la perdita o la trasformazione di protoni, neutroni o elettroni. C’è da dire anche che le particelle subatomiche hanno un forte legame con l’energia, anch’essa rilasciata dai decadimenti. Schrödinger pose un atomo a rischio di decadimento, come la zia un po’ appesantita, dal quale dipendeva l’accensione di un interruttore. Da questo interruttore sarebbe dipesa la vita del gatto. In ultima analisi quindi la sopravvivenza del felino dipendeva direttamente da un fenomeno quantistico. Questo fenomeno, definito da funzioni ondulatorie, è incerto fino a che non viene aperta la scatola, di conseguenza finché non viene rimosso il coperchio, il gatto può essere sia vivo che morto. Qui arriva il paradosso: come fa il gatto ad essere sia vivo che morto? All’epoca la spiegazione riscosse non poco successo e anche qualche critica, tra gli altri Heisenberg fu uno degli avversari più famosi di Schrödinger, con il quale ebbe non poche diatribe. Vivo o no, una volta uscito dalla scatola il gatto non sarebbe stato di certo grato a Schrödinger, ragion per cui questo è conosciuto come un esperimento mentale e non fu mai realizzato, per quanto ne sappiamo noi. Nel qual caso sarebbe stato meglio utilizzare un contenitore con dei fori per l’aria. Tra gli altri importanti contributi alla fisica Schrödinger scrisse l’equazione che porta il suo nome. Per i suoi studi di meccanica quantistica vinse il Nobel per la fisica nel 1933. Ebbe numerosi problemi con l’ascesa di Adolf Hitler, come molti altri suoi coevi. Benvoluto da molti dei suoi amici trovo rifugio anche in Italia, con l’aiuto di Enrico Fermi. Schrödinger morì il 4 gennaio del 1961, colpito dalla tubercolosi, rimasto uno degli ultimi di quella generazione di fisici che cambiò il mondo.

Chimica o Fisica? Questo è il dilemma
Per rispondere bisogna partire dalla definizione di chimica. La chimica è quella scienza che studia il comportamento dei materiali e delle sostanze e delle loro iterazioni tra di loro. Può sembrare poco detto così, ma letteralmente è chimica qualunque cosa ci circondi (tranne le fantomatiche scie rilasciate dagli aerei, sia chiaro). Già nella cultura greca, Democrito fu il primo a usare il termine àtomos, e romana, con Lucrezio e gli epicurei, si era consapevoli che la materia fosse composta di questi blocchi fondamentali e indivisibili, convinzione che si scoprì essere errata, ma ben poco si sapeva della loro natura. Con il 1700 e poi il 1800, dalla definizione di mole fino alle teorie su molecole e modelli atomici, il legame tra chimica e fisica, prima considerate alchimia e meccanica e per questo estranee, divenne palese. Le scoperte di Schrödinger, Bohr, De Broglie e altri, aprirono la strada alla chimica quantistica, branca della chimica teorica. Non c’è quindi una linea di demarcazione esatta dove finisce l’una e comincia l’altra. Prendiamo ad esempio il sale da cucina. Tutti dovrebbero sapere che si tratta di un solido cristallino, con formula NaCl. Guardiamolo dal punto di vista chimico: si tratta di un insieme di ioni sodio e ioni cloro, che posso ottenere ad esempio mescolando NaOH, soda caustica, e HCl, acido muriatico. Serve invece la fisica per spiegare la sua struttura e i legami tra i diversi atomi. Perché il sale ha proprio quella forma? Perché gli atomi stanno a quella distanza, né più vicini né più lontani? Semplice: gli atomi, un po’ come i magneti giocattolo, se messi troppo vicini si respingono. Da questo consegue che c’è una distanza a cui gli atomi preferiscono stare, un buon equilibrio tra attrazione e repulsione, che cambia da sostanza a sostanza. Questo ha chiaramente influenze sul comportamento chimico del materiale. Se poi facciamo sciogliere il sale in acqua e lo utilizziamo come elettrolita, parliamo di elettrochimica. E ancora quando andiamo a studiare il moto delle cariche all’interno di un fluido o di un filo sforiamo nell’elettromagnetismo e nella relatività. Ci basta pensare che molte scoperte di chimica sono state fatte da fisici e viceversa. Anche in ambito sperimentale queste due materie si intrecciano, ed è questo a renderle affascinanti. C’è anche da dire che quando si è cominciato a studiare gli atomi in modo approfondito osservare le interazioni chimiche tra due sostanze era fondamentale. Infine è d’obbligo citare la differenza tra proprietà chimiche e fisiche, che a volte possono ingannarci. Se immaginate di spruzzare, non fatelo a casa, dell’alcol etilico su un fornello acceso, saprete anche che il risultato è una fiamma non indifferente. Quello che forse non saprete, e di nuovo fidatevi e non fatelo a casa, è che lo stesso risultato si ottiene soffiando della farina. Quindi la farina è infiammabile? Oppure l’alcol prende fuoco solo sotto forma di goccioline? In questo caso la fiamma è dovuta a due motivazioni profondamente diverse. L’alcol è infatti una sostanza liquida a temperatura ambiente ed estremamente infiammabile. La farina invece “diffonde” il fuoco grazie al suo grado di suddivisione molto elevato, in altre parole grazie ai suoi granelli molto molto fini. La prima è una proprietà che ha a che fare con la composizione chimica, la seconda con la sua condizione fisica.

Un ingegnere volò sul nido del chimico
E cominciò a usufruire di tutte le sue scoperte. In particolare, per quanto riguarda il lavoro di Schrödinger, ogni ingegnere ha un debito nei suoi confronti. Basti pensare che gli ingegneri hanno a che fare letteralmente con qualunque forma di materia, la materia è formata da atomi, e Schrödinger di atomi ne sapeva parecchio. Dai computer quantistici, all’elettronica, alla scienza dei materiali, la meccanica di Schrödinger trova sempre più spazio nell’avanzare della tecnica. Le scoperte di scienziati come Einstein, Schrödinger, Planck e Bohr sono ormai insegnate in qualunque indirizzo di ingegneria e sono considerate fondamentali per la comprensione della chimica e della fisica. L’ingegneria chimica in particolare subisce gli influssi della termodinamica, che a sua volta è strettamente legata ai moti degli atomi e al loro comportamento. Tra i vari compiti dell’ingegnere chimico c’è il simulare e studiare da una parte grandi quantità di materia all’interno di reattori, dall’altra le proprietà e la struttura dei materiali. Per fare questo è necessario conoscere il comportamento degli atomi, in modo da poterlo generalizzare e creare dei modelli. Sia la chimica computazionale che la termodinamica statistica si occupano di questo, ma su due piani ben diversi. La prima ha infatti a che fare con singole molecole, la seconda invece prende in considerazione migliaia di moli di materia per creare dei modelli utili e attendibili. A livello ingegneristico c’è quindi un’approssimazione del modello quantistico. Sarebbe folle considerare ogni singolo atomo in un reattore che contiene tonnellate di liquido, è invece più utile guardare il comportamento dell’insieme. Questo non significa affatto che l’ingegnere si lavi le mani di quello che dice la meccanica quantistica, al contrario. La termodinamica infatti, come anche altre materie, generalizza, ampia e implementa, delle formule valide per l’immensamente piccolo, legandole con quello che noi vediamo e tocchiamo. Se poi guardiamo a un legame tra le particelle subatomiche e l’immensamente grande, nel tempo stanno avanzando sempre più teorie, quali quella della gravità quantistica, che si propongono di legare quanti e relatività. Ancora però nessuno è riuscito a dare prove della validità di questi modelli. In ultima analisi si può dire che non esiste nessuna branca della scienza scevra da legami con le altre. A volte l’istruzione italiana è in questo troppo pedante e molto teorica, ma forse l’idea di conoscere ciò che si cela dietro ai fenomeni e ciò che lega fisica, chimica, ingegneria, non è poi così sbagliata.