L’ONU ha proclamato il 2019 come l’International Year of the Periodic Table in occasione del centocinquantenario dell’intuizione geniale del chimico russo Mendeleev che ha rivoluzionato l’intero mondo scientifico.
La tavola periodica degli elementi è stata creata per la prima volta nel 1869 da Mendeleev il quale ordinò i composti chimici fino ad allora conosciuti secondo il loro peso atomico e in varie righe e colonne. Le sostanze individuate dal chimico avevano delle proprietà che, a intervalli regolari, si ripetevano nella stessa sequenza.
Cenni storici sulla tavola periodica
Nel 1869 Meyer e Mendeleev scoprirono in maniera indipendente che gli elementi, organizzati con la massa atomica crescente, portavano alla formazione di gruppi di sostanze caratterizzate da proprietà analoghe.
In particolare il chimico russo aveva intuito che ci fossero delle lacune nel suo sistema periodico, presumendo che gli elementi mancanti non erano stati ancora scoperti. La conferma giunse nel 1886 quando Clemens Winkler scoprì il germanio, che Mendeleev aveva previsto con il nome di ekasilicio.
Anatomia della tavola periodica
La tavola è suddivisa essenzialmente in quattro blocchi:s,p,d,f. Alcune eccezioni sono constatabili: ad esempio l’elio dovrebbe appartenere al gruppo s per la sua configurazione elettronica esterna mentre l’idrogeno, seppur possedendo un unico elettrone s, necessita di un solo altro elettrone per raggiungere la configurazione del gas nobile più vicino a lui nella tavola (e quindi può comportarsi in casi particolari da alogeno).
Il blocco d è quello dei metalli di transizione, caratterizzati da un graduale riempimento degli orbitali d. In questa variegata classe ritroviamo elementi quali il tungsteno (utilizzato per i filamenti delle lampadine a incandescenza), il ferro, il cobalto (i cui isotopi sono impiegati nell’ambito chemioterapico), il rame, l’oro e così molti altri.
Il gruppo f invece è caratterizzato dagli elementi che comunemente sono meno noti. La prima riga di questo blocco è detta dei lantanidi mentre la seconda degli attinidi. Gli elementi più conosciuti del blocco f sono certamente l’uranio e il plutonio, sostante coinvolte nella produzione di energia nucleare nonché di ordigni bellici per la distruzione di massa.

Proprietà chimiche periodiche degli elementi
La tavola periodica è utilizzabile per la previsione di numerose proprietà degli elementi, spesso fondamentali per la comprensione della chimica e del comportamento di date specie chimiche:
-
- Raggio atomico; è un dato definibile come la metà della distanza internucleare tra molecole biatomiche del composto in esame. Esso tende ad aumentare lungo il gruppo e a diminuire lungo il periodo. Ciò è dovuto al fatto che lungo il gruppo gli elettroni occupano orbitali sempre più lontani dal nucleo, risentendo sempre meno dell’interazione elettrostatica con i protoni, mentre lungo il periodo l’aumento degli elettroni non è compensato da una corrispettiva crescita delle dimensioni volumiche atomiche.

Calcolo del raggio atomico disponendo di molecole biatomiche del composto. In questo caso è raffigurata una molecola di H2. - Energia di ionizzazione; energia richiesta per allontanare un elettrone da una specie chimica neutra o carica elettricamente. In genere l’energia di ionizzazione primaria declina discendendo lungo un gruppo e aumenta lungo un periodo. E’ molto elevata per composti quali gli alogeni i quali, al contrario, tendono ad acquisire la configurazione dei gas nobili e non a perdere ulteriori elettroni. Al contrario, è molto bassa per i composti del gruppo 1s i quali, mediante la perdita di un elettrone, raggiungono la configurazione esterna otteziale del gas nobile che li precede nella tavola.
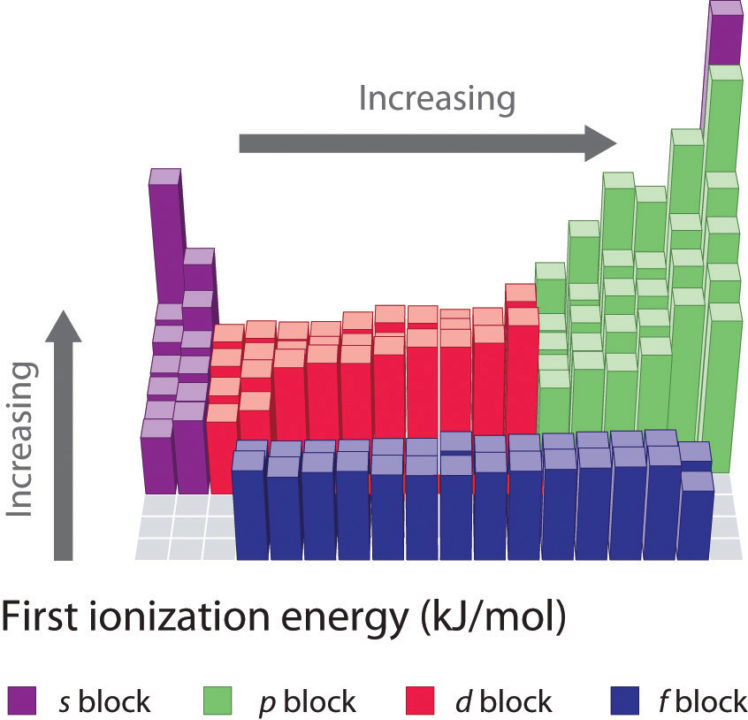
Trend dell’energia di ionizzazione sulla tavola periodica. - Affinità elettronica; energia liberata da un elemento quando un elettrone si lega a un suo atomo in fase gassosa. Per motivi analoghi a quelli descritti per l’energia di ionizzazione, per i metalli del blocco s essa ha un valore molto elevato mentre bisogna fornire molta energia ai gas nobili.

Trend dell’affinità elettronica sulla tavola periodica. - Elettronegatività; tendenza ad assumere su di sè gli elettroni di valenza durante la formazione di un legame chimico. Il valore massimo (ca. 4 sulla scala del Pauling) è posseduto dal fluoro mentre il valore minimo (ca. 0,8) è del cesio. Quando la differenza di elettronegatività tra le specie chimiche reagenti è diversa da zero si possono avere legami covalenti polari o perfino ionici a seconda dei casi.

Trend dell’elettronegatività sulla tavola periodica.
- Raggio atomico; è un dato definibile come la metà della distanza internucleare tra molecole biatomiche del composto in esame. Esso tende ad aumentare lungo il gruppo e a diminuire lungo il periodo. Ciò è dovuto al fatto che lungo il gruppo gli elettroni occupano orbitali sempre più lontani dal nucleo, risentendo sempre meno dell’interazione elettrostatica con i protoni, mentre lungo il periodo l’aumento degli elettroni non è compensato da una corrispettiva crescita delle dimensioni volumiche atomiche.
Roberto Parisi

