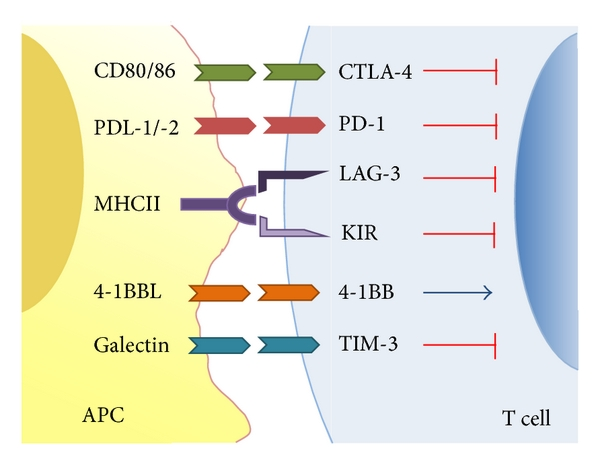
L’immunoterapia con inibitori di vari checkpoint cellulari è un’importante modalità del cancro, ma dei biomarker migliorati sono necessari per predire meglio come il paziente risponderà.
Gli approcci computazionali correnti che permettono di definire l’immunogenicità del tumore mediante l’analisi dettagliata dei campioni di tumore per contare le mutazioni e predire gli epitopi neoantigenici sono incapaci di considerare le variazioni clonali nei tumori.
Le sfide moderne dell’immunoterapia
La mancanza di responsività agli inibitori di checkpoint del ciclo cellulare è un problema centrale nell’era moderna dell’immunoterapia tumorale. I neoantigeni tumorali sono dei target critici della risposta immunitaria antitumorale dell’ospite e la loro presenza è correlata con l’efficacia del trattamento immunoterapico. Molti studi che prevedono l’analisi dei neoantigeni tumorali si focalizzano principalmente sull’intera carica neoantigenica, che in maniera semplicistica tratta tutti i neoantigeni allo stesso modo.
Il team del prof. Lu, ha pubblicato un articolo su Science Immunology col suo team il 21 febbraio 2020, dal titolo “Tumor neoantigenicity assessment with CSiN score incorporates clonality and immunogenicity to predict immunotherapy outcomes”, dove viene presentato un punteggio dell’Indice Cauchy-Schwarz dei Neoantigeni al fine di valutare il grado di concentrazione dei neoantigeni immunogenici nelle mutazioni troncali (ossia ancestrali, che avvengono nel tronco dell’albero filogenetico condiviso da tutti i cloni cellulari).
A differenza delle determinazioni della carica totale neoantigenica, CSiN incorpora gli effetti sia della clonalità che dell’affinità di legame a MHC dei neoantigeni quando si caratterizza il profilo tumorale. Analizzando le risposte cliniche in 501 pazienti oncologici trattati (la maggior parte ha ricevuto inibitori dei checkpoint del ciclo cellulare), è stato dimostrato che i punteggi CSiN predicono le risposte ai trattamenti per gli inibitori di checkpoint e la prognosi per pazienti affetti da melanoma, cancro ai polmoni e ai reni.
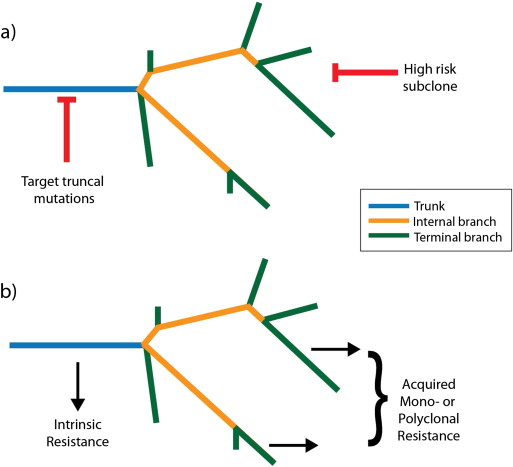
Costruire il punteggio CSiN
Alcune mutazioni somatiche sono troncali mentre invece altre sono subclonali. Le mutazioni troncali sono condivise tra più cloni tumorali differenti e, se presi di mira dalle cellule T mediante i neoantigeni, risulteranno in un effetto citotossico più forte. Le mutazioni subclonali sono differenti fra i singoli cloni e, se una mutazione subclonale è in un clone con una maggiore frazione clonale, i neoantigeni associati a tale mutazione avranno un effetto maggiore sulla sopravvivenza delle cellule tumorali rispetto alle mutazioni subclonali associate con cloni di minore frequenza. Ogni mutazione somatica potrebbe generare un differente numero di neoantigeni di varie lunghezze peptidiche (8-11 amminoacidi per i peptidi che si legano a MHC-1 e 15 amminoacidi per i peptidi che si legano a MHC-2) con differenti registri e presentati da differenti alleli HLA. Le inserzioni e le delezioni solitamente generano un maggiore numero di neoantigeni per mutazione rispetto a mutazioni missenso quando portano alla traduzione di segmenti completamente nuovi di sequenze proteiche. Si è pertanto ipotizzata una distribuzione favorevole dei neoantigeni e che le mutazioni tumorali avvengono quando i neoantigeni immunogenici sono concentrati sulle mutazioni troncali. Sulla base di queste premesse è stato sviluppato il punteggio CSiN per testare le predizioni.
Checkpoint cellulari e immunitari a confronto
Le cellule sane si muovono attraverso le fasi del ciclo cellulare in maniera strettamente regolata. Esse infatti utilizzano informazioni relative al loro stato interno e ricevono notizie dall’ambiente esterno per decidere quando e come proseguire con la divisione cellulare. Tale regolazione fa sì che le cellule non si dividano in condizioni sfavorevoli (es. DNA danneggiato o troppe cellule in un tessuto). Esistono vari checkpoint cellulari ma i tre più importanti sono:
- Checkpoint G1 = è il punto cruciale per una cellula, perché è qui che si decide se una cellula si deve dividere o meno. Una volta che la cellula passa il checkpoint, entra in fase S e il processo di divisione cellulare diviene irreversibile. Al checkpoint vengono valutate differenti caratteristiche, come la grandezza cellulare, la disponibilità di nutrienti, la presenza di specifici segnali molecolari e l’integrità degli acidi nucleici. Questi non sono gli unici fattori che possono influenzare la progressione della cellula attraverso il checkpoint e tutte quelle che non riescono a superarlo entrano in una fase di quiescenza nota come G0;
- Checkpoint G2 = la cellula possiede un ulteriore checkpoint proprio prima della fase M del ciclo cellulare, al fine di evitare sia danni al DNA sia che il processo di duplicazione semiconservativa sia andato a buon fine. Se vengono registrati degli errori, la cellula si arresta in questa fase per permettere la riparazione endogena. Qui, se il danno al DNA è irreparabile, può essere innescato il processo di apoptosi. Questo meccanismo di autodistruzione permette al DNA danneggiato di non essere trasferito alle cellule figlie, prevenendo la formazione di potenziali cellule tumorali;
- Checkpoint M = detto anche di fuso mitotico, permette alla cellula di valutare se i cromatidi fratelli hanno aderito in maniera corretta ai microtubuli del fuso. Siccome la separazione dei cromatidi in anafase è un processo irreversibile, il ciclo non procede finché tutti i cromosomi sono fermamente adesi ad almeno due fibre del fuso dai poli opposti della cellula.
La terapia a base di inibitori di checkpoint è uno dei mezzi più potenti dell’immunoterapia tumorale. La terapia prende come target i checkpoint immunitari, regolatori chiave del sistema immunitario. Alcune forme di cancro possono proteggersi da sole stimolando i target dei checkpoint immunitari. Nel 2011 è stato approvato il primo farmaco che prende di mira un checkpoint immunitario, ipilimumab, bloccante di CTLA4. Al giorno d’oggi sono approvati inibitori che colpiscono CTLA4, PD-1 (proteina transmembrana, nota come CD279, coinvolta nella morte cellulare programmata) e PD-L1 (ligando proteico di PD-1). PD-L1, esposto sulla superficie delle cellule, si lega a PD-1 esposto sulla superficie delle cellule immunitarie, inibendo l’attività di queste ultime. Tra le funzioni di PD-L1 vi è la regolazione delle attività dei linfociti T. Sembra che l’upregolazione (causata da fattori tumorali) di PD-L1 sulla superficie cellulare inibisca le cellule T che, in condizioni normali, attaccherebbero le cellule mutate. Pertanto gli anticorpi che si legano a PD-1 o a PD-L1 bloccano l’interazione permettendo ai linfociti T di attaccare le cellule tumorali.