In un articolo pubblicato su Nature il 29 Gennaio, gli scienziati hanno dimostrato che gli organoidi, detti solitamente mini-brains, non corrispondono esattamente ai cervelli in vivo.
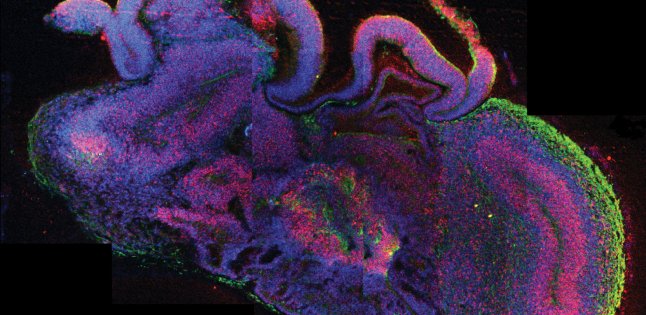
Il professor Kriegstein, assieme al suo team di ricercatori, ha identificato i geni attivi in 235.000 cellule estratte da 37 differenti organoidi e li ha comparati con quelli provenienti da 189.000 cellule estratte da cervelli normali in via di formazione.
Cos’è un organoide?
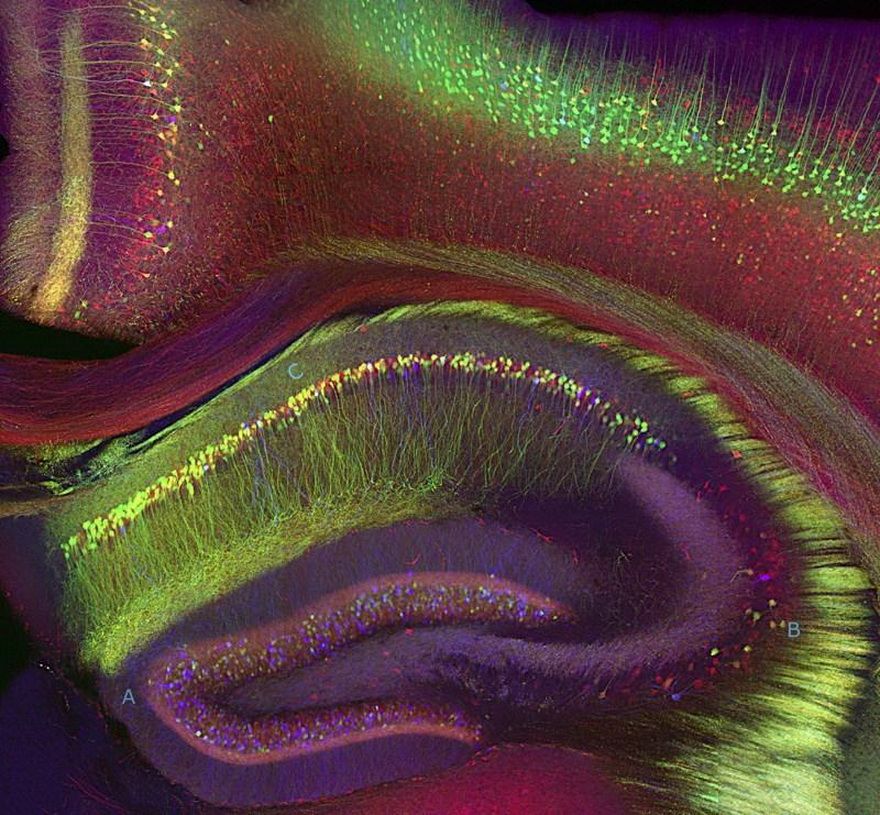
Gli organoidi cerebrali sono ammassi di cellule staminali che sono trasformate da un tipo all’altro finché non divengono neuroni o altri tipi di cellule mature. Secondo l’articolo pubblicato su Nature dal team del prof. Kriegstein, intitolato “Cell stress in cortical organoids impairs molecular subtype specification”, le staminali possono anche non completare del tutto il loro processo di maturazione e differenziamento. Pertanto, siccome sono presenti ancora delle cellule immature da un punto di vista fenotipico, non si viene a ricreare la normale struttura organizzativa cerebrale. Ciò potrebbe rappresentare un problema per tutte quelle malattie neurologiche e neurodegenerative quali la schizofrenia o l’Alzheimer che sono spesso riferite a specifiche cellule e circuiti neuronali. Molte cellule degli organoidi cerebrali mostrano segni di stress metabolico per cui le comune condizioni di coltura cellulare non corrispondono a quelle di un cervello che si sta sviluppando normalmente. Kriegstein ritiene tuttavia che le strutture organoidi siano ancora valide per spiegare e comprendere il funzionamento di relativamente ristretti cluster di neuroni, ma tiene a mettere in guardia tutti gli scienziati che desumono aspetti tipici dell’intera corteccia cerebrale a partire da queste strutture modello create artificialmente in laboratorio.
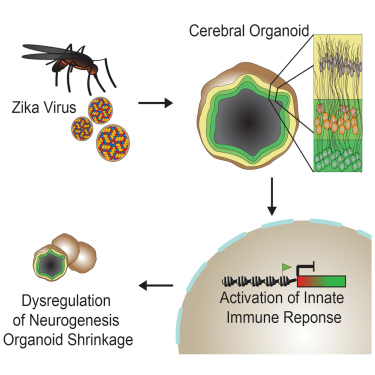
Esempi di usi fondamentali degli organoidi cerebrali provengono da studi sul virus Zika, in cui si è dimostrato un nesso di causalità fra esposizione all’agente virale di donne gravide e alle ridotte dimensioni cerebrali dei neonati in seguito al processo ontogenico embrionale. Molti altri scienziati di tutto il mondo continuano ad utilizzare tali colture cellulari per analizzare eventuali farmaci o droghe ad effetto dipendente, per comprenderne i meccanismi molecolari e l’efficacia in ambito anestetico e farmacologico. Altri esperti, come Sergiu Pasca, vedono nella scoperta di Kriegstein un punto di partenza per l’analisi dell’onset di differenti malattie neurodegenerative siccome si verificano le stesse condizioni di stress che portano ad una patologia di quel tipo.
Un’applicazione degli organoidi cerebrali: il virus Zika
Negli anni 2015-2016 vi fu un’epidemia virale dovuta all’agente ZIKV, un flavivirus presente nei moscerini. Negli adulti l’infezione risulta nella manifestazione semeiotica di sintomi lievi mentre vi è una maggiore incidenza di neonati con la microcefalia, una condizione in cui i pazienti nascono con una testa anormalmente piccola. Sin da quando l’epidemia del virus Zika è stata considerata un’emergenza sanitaria globale dall’OMS, sono stati condotti numerosi studi clinici su tessuti fetali microcefalici che hanno mostrato la presenza di ZIKV nei cervelli fetali danneggiati.
In molti esami come quelli descritti precedentemente, sono stati selezionati gli organoidi cerebrali perché essi permettono di iniettare il virus in tutte le regioni che “simulano” il cervello in vivo e permette agli scienziati di comprendere come tale agente infettivo si comporti con le differenti popolazioni neurali presenti in un cervello in via di sviluppo come quello di un neonato.
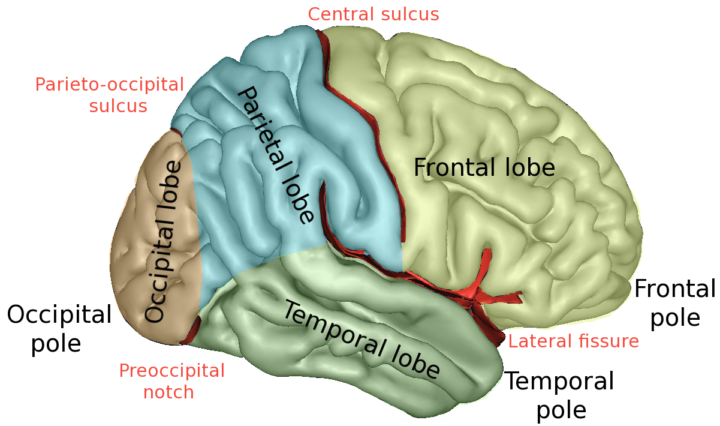
Cenni sulla struttura neocorticale umana
La struttura più craniale del sistema nervoso centrale umano è rappresentata dalla neocortex, composta da popolazioni neurali di differente tipo che determinano differenti pattern microscopici i quali vengono distinti grazie alla branca della citoarchitettura. Esistono dei solchi principali, tra i quali ricordiamo quello centrale di Rolando, che separa superomedialmente il lobo frontale da quello parietale, quello laterale di Silvio, che separa strutture quali il giro frontale inferiore dagli elementi del giro temporale superiore (ed internamente copre l’insula) e uno posteriore, detto scissura calcarina, che rappresenta la sede della area di Brodmann 17 corrispondente alla corteccia visiva primaria, dove arrivano i neuroni provenienti dalla radiazione ottica lungo i tratti genicolocalcarini.