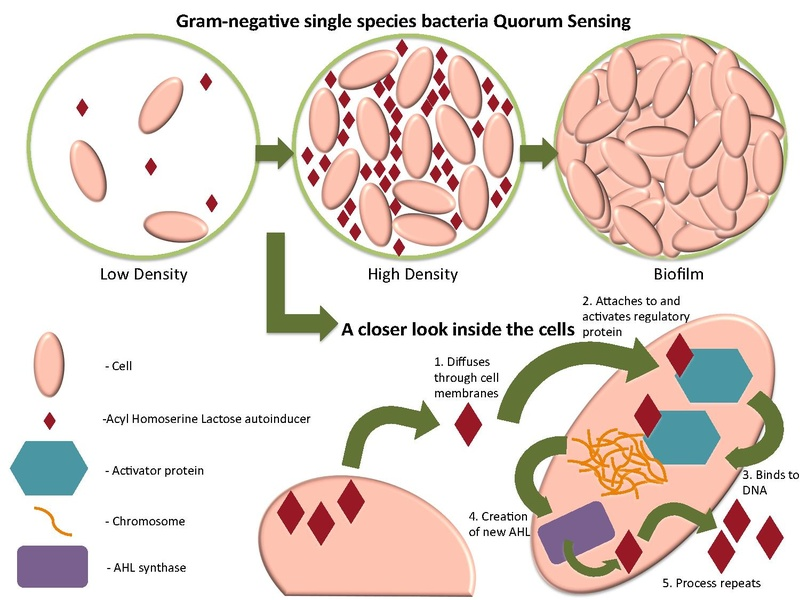
Come con un gioco di squadra ,attraverso il quorum sensing I batteri si coordinano nell’esercitare una loro capacità per ottenere un risultato.

Quanto assomigliano le strategie batteriche di quorum sensing alle tattiche della falangi del mondo antico o anche solo banalmente alle strategie dei branchi di lupi?
Questi usano in combinazione l’espressione di geni attivandoseli gli uni gli altri al fine di coordinare un’azione di gruppo.
Tattiche di gruppo:
C’è stato un momento nella storia della strategia militare dove ci siamo accorti di quanto il lavoro coordinato di un certo numero di persone era più efficace del lavoro dei singoli abbiamo iniziato a sviluppare varianti di strategie dove gli uni gli altri ci si poteva difendere anche dai danni a distanza e contemporaneamente infliggere in maniera implacabile più danni possibili.

Una tra tutte la falange macedone che rappresentò il culmine della strategia della falange prima del manipolo della legione romana.
Il tutto è finalizzato al salvaguardare i compagni con gli ampi scudi e contemporaneamente garantire al nemico la possibilità di essere infilzato sulla media, lunga e corta distanza, grazie alla sovrapposizione delle sarisse.
Negli animali si trovano tattiche di gruppo altrettanto efficaci, anche se ovviamente meno elaborate.

O ancora la banale sovrapposizione contemporanea di forze può permettere ad una branco di iene di sopraffare un avversario temibile come un leone, attaccandolo con il classico mordi e fuggi dai punti ciechi.

Se scendiamo ancora più di dimensioni troviamo il caso del fenomeno del quorum sensing.
L’unione fa l’intossicamento:
Il quorum sensing è la regolazione dell’espressione genica in risposta alle fluttuazioni della densità della popolazione cellulare. I batteri sensibili al quorum producono e rilasciano molecole di segnale chimico chiamate autoinduttori che aumentano la concentrazione in funzione della densità cellulare. Il rilevamento di una concentrazione stimolante soglia minima di un autoinduttore porta ad un’alterazione nell’espressione genica.
I batteri Gram-positivi e Gram-negativi usano circuiti di comunicazione con rilevamento del quorum per regolare una vasta gamma di attività fisiologiche. Questi processi includono simbiosi, virulenza, competenza, coniugazione, produzione di antibiotici, motilità, sporulazione e formazione di biofilm. In generale, i batteri Gram-negativi usano i lattoni di omoserina acilati come autoinduttori, e i batteri Gram-positivi usano i peptidi di oligo elaborati per comunicare.
I recenti progressi nel campo indicano che la comunicazione cellula-cellula tramite autoinduttori avviene sia all’interno che tra le specie batteriche. Inoltre, ci sono dati crescenti che suggeriscono che gli autoinduttori batterici suscitano risposte specifiche dagli organismi ospiti. Sebbene la natura dei segnali chimici, i meccanismi di trasmissione del segnale e i geni target controllati dai sistemi di rilevamento del quorum batterico differiscano, in ogni caso la capacità di comunicare tra loro consente ai batteri di coordinare l’espressione genica, e quindi il comportamento, del intera comunità.
Presumibilmente, questo processo conferisce ai batteri alcune delle qualità degli organismi superiori. L’evoluzione dei sistemi di rilevamento del quorum nei batteri avrebbe potuto quindi essere uno dei primi passi nello sviluppo della multicellularità.

Ma come avviene l’attivazione genica nei batteri? cosa c’entrano queste molecole secrete con l’attivazione di interi pathway biochimici batterici?
Gli operoni e i reguloni:
Un esempio di regolazione la troviamo per esempio nel buon vecchio Escherichia coli.
In una cellula batterica alcune proteine vengono prodotte a ritmo costante, perché sono sempre necessarie; altre invece vengono prodotte solo quando il batterio ne ha bisogno. In questo caso la cellula dimostra di riconoscere una variazione chimica dell’ambiente esterno e di saper attivare o bloccare i suoi geni in relazione alla nuova situazione.
Il metabolismo del lattosio in Escherichia coli è un buon esempio per descrivere questa capacità di adattamento. Essendo un normale inquilino dell’intestino umano, E. coli deve essere capace di adattarsi agli improvvisi cambiamenti del suo ambiente. Il suo ospite può metterlo in contatto con un certo tipo di cibo e, poche ore dopo, con uno totalmente diverso. Queste variazioni costituiscono una sfida metabolica per il batterio.
La fonte di energia preferita da E. coli è il glucosio, lo zucchero più facile da metabolizzare, ma non tutto il cibo ingerito dall’ospite contiene un’elevata quantità di glucosio. Per esempio, il batterio può trovarsi improvvisamente sommerso dal latte, che contiene lo zucchero lattosio. Il lattosio è un disaccaride contenente una molecola di galattosio legata a una molecola di glucosio. Per essere assorbito e metabolizzato da E. coli, il lattosio deve subire l’azione di tre proteine, di cui una (chiamata β-galattosidasi) è un enzima che catalizza la scissione del legame tra i due monosaccaridi.
Quando E. coli cresce su un terreno contenente glucosio ma privo di lattosio, i livelli di queste tre proteine sono estremamente bassi: ovvero i geni che le codificano sono «repressi», cioè inattivi. Se però l’ambiente cambia e il lattosio diventa lo zucchero più abbondante, il batterio si affretta a produrre tutte e tre le proteine. Quindi i geni che codificano per queste proteine vengono attivati, cioè trascritti e tradotti; di conseguenza la concentrazione delle proteine nella cellula aumenta rapidamente.
In una cellula di E. coli che cresce su un terreno privo di lattosio si trovano soltanto due molecole di β-galattosidasi; la presenza di lattosio, invece, può indurre la sintesi di 3000 molecole di β-galattosidasi per ogni cellula!
Se dal terreno di coltura di E. coli si toglie il lattosio, la sintesi di β-galattosidasi si arresta quasi subito. Le molecole di enzima già prodotte non scompaiono, semplicemente si diluiscono nel corso delle successive divisioni cellulari finché la loro concentrazione all’interno di ogni cellula batterica ridiscende al livello iniziale. 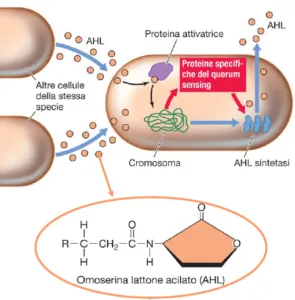
I geni che codificano i tre enzimi coinvolti nel metabolismo del lattosio di E. coli vengono definiti geni strutturali, a indicare che specificano la struttura primaria (cioè la sequenza amminoacidica) di una proteina; in altre parole, sono geni trascrivibili in mRNA.
Più operon attivati in seguito (potremmo dire in serie usando un termine di elettrostatica legato alle resistenze ed i circuiti abbastanza fuori luogo)
costituiscono l’unità funzionale del regulone che altro non è che il meccanismo in toto del pathway biochimico.
Attraverso queste strategie i batteri riescono rilasciando determinate molecole ad attivare vie biochimiche non trasducendo solo loro stessi il segnale, ma facendolo trasdurre anche ai membri del film batterio vicini.
In questo modo magari attiveranno tutti insieme il rilascio di tossine per esempio, dando il via ad un vero e proprio bombardamento biochimico sui tessuti malcapitati.